
PROPIEDADES DE LA MATERIA
EXTERNAS: Nos permiten diferenciar la forma, su composición, tamaño, masa, peso, inercia, impenetrabilidad.
INTERNAS: color, sabor, olor, densidad, punto de fusión, ebullición, dureza, maleabilidad, conductividad, térmica o eléctrica, solubilidad.
QUÍMICAS: Oxidación, Fotosíntesis, reacciones de oxidación o reducción.
PROCESOS FISICOS: Ejemplo la Fusión del agua
PROCESOS QUÍMICOS: Ejemplo la COMBUSTIÓN C + O2 --à CO2 + Energía
CONCEPTOS
ü EN LOS PROCESOS FÍSICOS NO HAY VARIACIÓN DE LA COMPOSICIÓN DE LA MATERIA, EL PROCESO ES REVERSIBLE.ü EN EL PROCESO QUÍMICO SI HAY VARACIÓN DE LA COMPOSICIÓN DE LA MATERIA, EL PROCESO ES IRREVERSIBLE.
ü EN LOS PROCESO QUÍMICOS HAY CAMBIOS ENERGÉTICOS, EN LOS FÍSICOS NO. LA REACCIÓN PUEDE SER EXOTÉRMICA CUANDO SE LIBERA Y ENDOTÉRMICA CUANDO ABSORVE ENERGÍA.
FORMAS DE LA MATERIA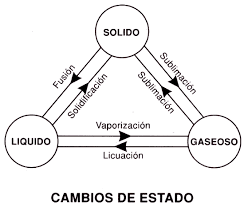
ELEMENTO: Sustancia formada por átomos de la misma clase, que no se puede descomponer. Ejemplo O2
COMPUESTO: Combinación de dos o más elementos.
SOLUCION: Unión de dos más sustancias formando una fase HOMOGÉNEA, además de composición variable.
Mol (n): g de la sustancia dada
PROBLEMAS:
1. Calcular la densidad del alcohol etílico C2H5 OH sabiendo que 8 mL pesan 64g.
2. La densidad del ácido sulfúrico H2SO4 es de 1, 84 g/ mL calcular la masa de 60 mL de ácido.
3. Calcular la densidad de un disco de bronce de 2,5 cm de diámetro y 8mm de espesor, el disco pesa 34,5 gr.
4. La densidad de un cilindro de aluminio de masa 75,21 g, diámetro 1,5 cm, y altura 15,75 cm.
5. Convertir 33°C a °K y °F.
6. Convertir 5°K a °C y °F .
7. Calcular el número de Moles de átomos de hay en 5g de Oxígeno.
9. Cuantas moles hay en 20g de ácido fosfórico H3PO4.
10. Cuantas moles hay en 5,7 g de Ca CO3.